Contente
- Principal diferença
- Gráfico de comparação
- O que são compostos iônicos?
- O que são compostos moleculares?
- Compostos Iônicos vs. Compostos Moleculares
Principal diferença
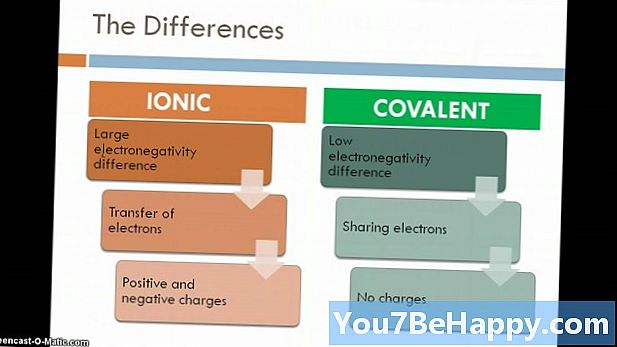
O composto é reconhecido como uma substância formada quando dois ou mais elementos se combinam em proporções definidas através de uma ligação química. O composto iônico é o composto formado devido à força de atração eletrostática entre os metais e os não metais. Geralmente, os compostos iônicos aparecem em um estado cristalino vendido. Além disso, os compostos iônicos são bons condutores de eletricidade e têm altos pontos de fusão e ebulição. Por outro lado, compostos moleculares são formados devido ao compartilhamento de elétrons entre dois não metais. Em relação ao composto iônico, eles são um mau condutor de eletricidade e possuem baixo ponto de fusão e ebulição.
Gráfico de comparação
| Compostos iónicos | Compostos Moleculares | |
| Formação | Os compostos iônicos são formados devido à força de atração eletrostática entre metais e não metais. | Os compostos moleculares são formados devido ao compartilhamento de elétrons entre dois não metais. |
| Grupo | Os compostos iônicos são formados entre metal e não mental. | Os compostos moleculares são formados quando dois não metais combinam quimicamente |
| Vinculo | O composto iônico é formado devido à força de atração eletrostática conhecida como ligação iônica. | Os compostos moleculares são formados devido à ligação covalente entre os elementos. |
| Ponto de fusão e ebulição | Alto | Baixo |
| Estado | Os compostos iônicos estão sempre em estado sólido com formação de aparência cristalina. | Os compostos moleculares podem estar em qualquer estado, sólido, líquido ou gás à temperatura ambiente. |
| Condutor de Eletricidade | Boa | Ruim |
O que são compostos iônicos?
Estes compostos são formados devido à força de atração eletrostática entre metais e não metais. Em palavras mais simples, a força (ligação iônica) nisto faz com que cargas positivas e negativas reajam em conjunto para formar um composto. Geralmente, os compostos iônicos aparecem em um estado cristalino vendido e são bons condutores de eletricidade, com altos pontos de fusão e ebulição. Os compostos iônicos são formados entre metais e não metais e têm algum tipo de aparência brilhante.
Exemplo: O sal de mesa (NaCl) é o exemplo mais comum de composto iônico. Nesta formação, o sódio (NA) é metal, enquanto o cloro (Cl) não é metal, ambos são mantidos juntos devido à força eletrostática da atração entre os dois.
O que são compostos moleculares?
Os compostos formados devido ao compartilhamento de elétrons entre os não-metais são conhecidos como composto molecular. Os elementos que reagem aqui são mantidos juntos devido à ligação covalente, e é por isso que esses compostos são frequentemente referidos como compostos covalentes.Em relação ao composto iônico, eles são um mau condutor de eletricidade e possuem baixo ponto de fusão e ebulição.
Exemplo: No ozônio (O3), o oxigênio combina com o compartilhamento de elétrons para formar o ozônio.
Compostos Iônicos vs. Compostos Moleculares
- Os compostos iônicos são formados devido à força de atração eletrostática entre metais e não metais, enquanto que os compostos moleculares são formados devido ao compartilhamento de elétrons entre dois não metais.
- Os compostos moleculares são formados quando dois não metais combinam quimicamente, por outro lado, compostos iônicos são formados entre metal e não mental.
- Os compostos moleculares são formados devido à ligação covalente entre os elementos, enquanto o composto iônico é formado devido à força de atração eletrostática conhecida como ligação iônica.
- Os compostos moleculares têm baixo ponto de fusão e ebulição em comparação com os compostos iônicos.
- Os compostos moleculares podem estar em qualquer estado, sólido, líquido ou gás à temperatura ambiente, enquanto que os compostos iônicos estão sempre em estado sólido com formação de aparência cristalina.
- Os compostos moleculares são maus condutores de eletricidade, enquanto os compostos iônicos são bons condutores de eletricidade.


